LysA Universal PARylation检测试剂盒:细胞总PARylation精准定量检测
- 武汉艾美捷科技有限公司2026年4月8日 2:42 点击:86
LysA Universal PARylation检测试剂盒:细胞总PARylation精准定量检测方案
在细胞应激响应与DNA损伤修复研究中,PARylation(多聚ADP-核糖化)作为一种关键的可逆翻译后修饰,正日益受到广泛关注。由PARP家族(PAR聚合酶)和PARG(PAR糖水解酶)共同调控的PAR稳态,在炎症、缺血、卒中及癌症等多种疾病进程中发挥着重要作用。针对PARP的抑制剂已在肿瘤治疗中获得成功,而PARG的过度表达与乳腺癌的发生发展密切相关。因此,准确、便捷地检测细胞内的总PARylation水平,对于基础研究及药物开发具有重要意义。由艾美捷代理BPS Bioscience研发的LysA Universal PARylation检测试剂盒(货号:82123)正是为此设计的一套完整的酶联免疫吸附测定(ELISA)解决方案。
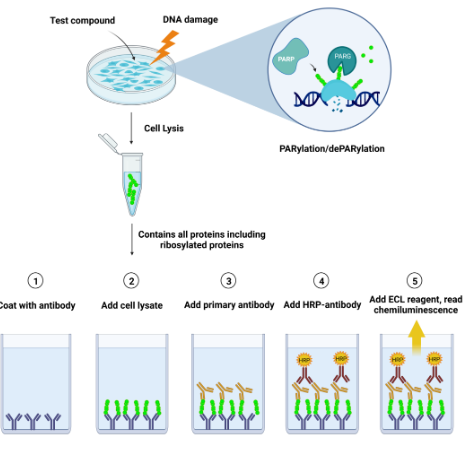
图1:LysA通用PAR化检测工作流程图。
使用抗标准杆数(PAR)抗体包被96孔板。将细胞裂解液加入包被的孔中,使细胞裂解液中的标准杆数(PAR化蛋白)被抗体捕获。随后与抗标准杆数一抗和HRP标记的二抗孵育。加入化学发光HRP底物后产生发光信号,该信号与细胞提取物中标准杆数的含量直接相关。
一、核心原理与检测性能
该试剂盒采用夹心ELISA原理,专用于定量检测细胞提取物中的总多聚ADP-核糖化水平。其独特之处在于提供了PAR标准品,用户可据此建立标准曲线,实现绝对定量。检测范围经验证在100 pM至20 nM PARylation区间内呈良好线性关系,确保了实验结果的精确性与可重复性。
试剂盒采用96孔板形式,包含实验所需的全部核心组分:特异性抗体、封闭缓冲液、检测试剂以及作为质控的细胞裂解物。这种“开箱即用”的设计极大简化了实验流程,减少了因自行配制试剂引入的批次间差异。
二、适用场景与主要应用
该试剂盒主要面向以下三类核心应用场景:
1. 培养细胞中总PAR水平的定量分析:研究人员可直接处理贴壁或悬浮培养细胞,裂解后利用试剂盒测定不同处理条件下细胞内PARylation的总体变化。
2. PARP或PARG抑制剂在细胞中的IC50测定:在药物筛选过程中,通过梯度处理候选化合物,可便捷计算出抑制剂的半数抑制浓度,为构效关系研究提供关键数据。
3. 细胞模型中PARP或PARG抑制剂的药效验证:除单纯的活性测定外,该试剂盒还可用于评估抑制剂在真实细胞环境中的作用效果,验证其是否如预期般降低PARylation水平,从而关联到细胞表型变化。
三、操作流程与所需配套材料
尽管试剂盒提供了核心检测试剂,用户仍需自行准备以下关键辅助材料以获得最佳结果:
改良RIPA裂解液(中强度)(BPS Bioscience 82126):用于充分提取细胞蛋白,同时维持PAR修饰的稳定性。
LysA蛋白酶抑制剂混合物试剂盒(BPS Bioscience 82199):防止蛋白降解,保证检测准确性。
ADP-核糖化循环抑制剂混合物(82130)或完全ADP-核糖化循环抑制剂混合物(82539):这两项尤其重要——由于细胞内存在动态的PAR合成与降解循环,加入抑制剂可“冻结”取样瞬间的PARylation真实水平,避免在样品处理过程中因内源性PARG或ARH3活性导致信号衰减。
基本操作流程包括:细胞接种与药物处理 → 裂解液(含抑制剂)裂解 → 蛋白定量 → 加入预包被板孵育 → 检测抗体结合 → 化学发光底物显色 → 酶标仪读数 → 依据标准曲线计算PAR浓度。
四、存储稳定性与运输条件
试剂盒采用-80°C超低温运输,所有组分在收货后按指示存储条件下,自收货之日起6个月内保持最佳性能。用户需特别注意:反复冻融可能降低试剂活性,建议首次解冻后分装保存。
五、注意事项与局限性
特异性:该试剂盒仅检测多聚ADP-核糖化(PARylation),无法识别单ADP-核糖化(MARylation)。若研究重点为单修饰,需选择其他专用工具。
线性范围:严格控制在100 pM–20 nM范围内定量。超出该范围的高浓度样本需进行适当稀释后重新测定。
物种兼容性:试剂盒设计基于人源细胞体系,但在模式生物(如小鼠、大鼠)细胞中的交叉反应性需用户自行验证。
六、文献参考
Marques M., et al., 2019 Oncogene 38 (12): 2177-2191.
James D. I., et al., 2016 ACS Chem Biol 11 (11): 3179-3190.
Drown B. S., et al., 2018 Cell Chem Bio 25 (12): 1562-1570.
SARM1荧光检测试剂盒(水解酶活性):高通量SARM1 NADase活性筛选试剂盒
在神经退行性疾病研究中,SARM1(含无菌α和TIR基序的蛋白1)正成为一个备受关注的药物靶点。作为Toll/白细胞介素受体-1(TIR)家族的成员,SARM1具有ADP-核糖环化酶和NAD⁺糖水解酶活性,能够将NAD⁺切割为ADPR(ADP-核糖)、cADPR和烟酰胺。该蛋白高表达于神经元中,当受到损伤或代谢应激时,SARM1激活导致轴突内NAD⁺耗竭,进而触发病理性轴突丢失——这一过程被称为Wallerian变性。近年研究发现,人类SARM1基因的功能获得性突变与肌萎缩侧索硬化症(ALS)相关,而敲除或抑制SARM1活性则能在脑损伤或药物诱导的神经损伤模型中保护轴突。因此,开发高效、可靠的SARM1活性检测方法,对于筛选潜在抑制剂及机制研究至关重要。
由艾美捷代理的BPS Bioscience推出的SARM1 Fluorogenic Assay Kit (Hydrolase Activity)(货号:78217),正是为满足上述需求而设计的一整套荧光法检测试剂盒。以下从核心原理、试剂盒组分、适用场景及操作要点等方面进行详细介绍。
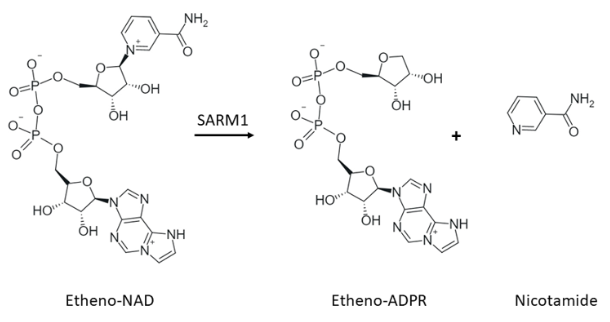
图1:测定原理。
SARM1的水解酶活性是通过监测Etheno-NAD水解形成Etheno-ADPR+烟酰胺的过程来测量的。由于内部猝灭作用,Etheno-NAD本身不具有荧光性。当SARM1对其进行水解时,会释放出烟酰胺,从而使荧光信号增强,且荧光信号的增强与酶活性直接成正比。
一、检测原理与核心优势
本试剂盒采用荧光底物N⁶-乙烯-NAD⁺(e-NAD),该底物为天然NAD⁺的类似物。在重组人源SARM1酶(氨基酸28-724)的催化下,e-NAD被水解生成乙烯-ADP-核糖和烟酰胺。与天然反应产物不同,乙烯-ADP-核糖在特定波长激发下会发出强烈荧光(激发/发射波长约为300/410 nm)。通过实时监测荧光强度的增加速率,即可直接反映SARM1的水解酶活性。
相较于传统的HPLC或比色法,荧光法具有以下显著优势:
实时动态监测:无需终止反应,可连续读取动力学曲线。
灵敏度高:检测下限可达亚微摩尔级别。
操作简便:均相“混合-读取”模式,无需分离步骤。
高通量兼容:支持96孔和384孔板,适用于自动化筛选。
二、试剂盒组分与存储稳定性
该试剂盒提供两种规格(96次反应或384次反应),每个试剂盒包含以下核心组分:
重组人SARM1酶(28-724氨基酸,活性蛋白)
荧光底物e-NAD
SARM1检测缓冲液
阳性对照抑制剂DSRM-3716:用于验证实验体系及计算抑制率
所有组分在收货后按指示条件存储(通常为-80°C),自收货之日起6个月内保持最佳性能。用户需注意避免反复冻融,建议首次解冻后分装保存。
三、适用应用场景
本试剂盒主要面向两大应用方向:
1. 小分子抑制剂的筛选与IC50测定
在药物发现流程中,研究者可通过本试剂盒对化合物库进行初筛,快速识别具有SARM1抑制活性的先导化合物。试剂盒提供的DSRM-3716可作为阳性对照,便于计算待测化合物的相对抑制率。典型的384孔板筛选方案可在30分钟内完成酶反应与读数。
2. 酶动力学研究
通过改变底物浓度或酶浓度,可测定SARM1的动力学参数,如Kₘ、Vₘₐₓ及k_cat。这对于理解突变体(如ALS相关突变)的催化特性或比较不同抑制剂的作用模式(竞争性、非竞争性等)具有重要意义。
四、实验流程简要说明
1. 试剂准备:将SARM1酶、e-NAD底物及缓冲液置于冰上解冻,平衡至室温。
2. 反应体系构建(以96孔板为例):每孔加入适量SARM1酶(通常为0.5–2 μg)与检测缓冲液,加入待测化合物或DMSO对照,预孵育5–10分钟。
3. 启动反应:加入e-NAD底物至终浓度(例如100 μM),立即置于荧光酶标仪中读数。
4. 数据采集:在激发300 nm/发射410 nm处,每1–2分钟读取一次,连续监测30–60分钟。反应速率(RFU/min)与酶活性成正比。
5. 数据分析:将抑制剂组的初始速率与对照组比较,计算抑制率及IC₅₀。
五、注意事项与配套建议
物种特异性:该试剂盒基于人源SARM1(hSARM1)设计,若研究小鼠或大鼠SARM1,需验证交叉反应性。
底物稳定性:e-NAD对光敏感,建议避光操作。
阳性对照:首次使用强烈建议运行DSRM-3716的剂量-响应曲线,以确认试剂盒及仪器状态。
辅助材料:用户需自行准备黑色/不透明底部的96或384孔板、多通道移液器及具备动力学读数功能的荧光酶标仪。
六、文献参考
Marques M., et al., 2019 Oncogene 38 (12): 2177-2191.
James D. I., et al., 2016 ACS Chem Biol 11 (11): 3179-3190.
Drown B. S., et al., 2018 Cell Chem Bio 25 (12): 1562-1570.
PARPtrap PARP2检测试剂盒:均相、免洗、高通量
在肿瘤治疗领域,PARP抑制剂已取得显著成功,其作用机制不仅在于抑制PARP酶的催化活性,更关键的是将PARP蛋白“捕获”在DNA损伤位点,形成致命的PARP-DNA复合物,导致癌细胞死亡。然而,第一代PARP抑制剂主要靶向PARP1,对PARP2的选择性及捕获效应研究相对不足。随着研究发现PARP2在前列腺癌等恶性肿瘤中过表达,并通过FOXA1/AR通路参与疾病进展,开发能够特异性诱导PARP2-DNA捕获的小分子抑制剂成为新的药物发现方向。
由艾美捷代理的BPS Bioscience推出的PARPtrap Assay Kit for PARP2(货号:78296),正是为高通量筛选和表征PARP2捕获型抑制剂而设计的完整解决方案。该试剂盒采用荧光偏振(Fluorescence Polarization, FP)技术,在均相体系中实时检测PARP2与DNA的结合状态,可快速评估化合物促进PARP2-DNA复合物形成的能力。以下从检测原理、试剂盒组分、应用场景及操作要点等方面进行详细介绍。
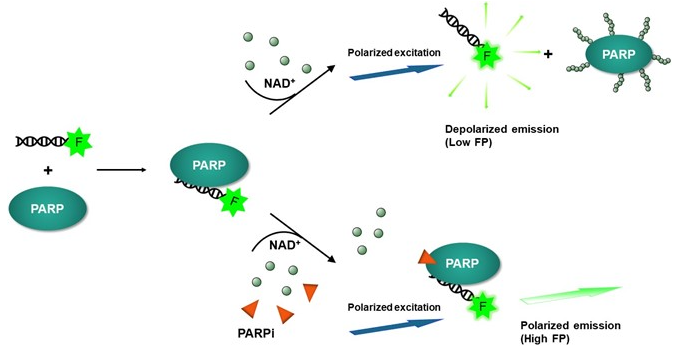
图1:测定原理。
SARM1的水解酶活性是通过监测Etheno-NAD水解形成Etheno-ADPR+烟酰胺的过程来测量的。由于内部猝灭作用,Etheno-NAD本身不具有荧光性。当被SARM1水解时,烟酰胺被释放出来,导致荧光信号增强,且荧光信号的增强与酶活性直接成正比。
一、检测原理:荧光偏振法监测PARP2-DNA相互作用
荧光偏振技术基于小分子在溶液中的旋转速度与其分子量之间的关系。当荧光标记的小分子(如寡核苷酸探针)处于自由状态时,旋转速度快,发射光偏振程度低;当该分子与较大的蛋白质(如PARP2)结合后,复合物旋转速度减慢,发射光偏振程度显著升高。
本试剂盒的核心设计如下:
1. 荧光标记的DNA双链探针:提供一条末端带有荧光基团(如FAM)的双链寡核苷酸,模拟DNA损伤位点的结构。
2. 重组人源PARP2酶(氨基酸2-583):包含完整的DNA结合域及催化域,具有NAD⁺依赖性自身核糖基化活性。
3. NAD⁺:作为PARP2的底物,在未添加抑制剂时,PARP2结合DNA后会发生自身PARylation,负电荷积累导致其从DNA上解离。
4. 待测化合物:若化合物具有“捕获”功能,则会阻止PARP2从DNA上解离,使其稳定结合在DNA探针上。
检测流程:将PARP2酶、荧光DNA探针、NAD⁺及待测化合物混合孵育。在无捕获剂时,PARP2结合DNA后迅速发生自身修饰并解离,荧光偏振值较低;在存在捕获型抑制剂时,PARP2被锁定在DNA上,形成高分子量复合物,荧光偏振值显著升高。通过测定偏振值(mP)的变化,即可量化化合物的捕获活性。
二、试剂盒组分与规格
该试剂盒提供两种规格:96孔板形式(100次反应)和384孔板形式(400次反应),每个试剂盒包含:
重组人PARP2酶(2-583氨基酸,纯度及活性经质控验证)
荧光标记的寡核苷酸双链(避光保存)
NAD⁺(需按说明溶解使用)
PARPtrap 检测缓冲液(优化了离子强度及pH,确保最佳结合效率)
详细操作说明书
所有组分在收货后按指示存储(通常为-80°C),自收货之日起6个月内保持最佳性能。荧光探针对光敏感,建议分装后避光保存,避免反复冻融。
三、核心应用场景
本试剂盒主要面向两大药物发现需求:
1. 高通量筛选(HTS)促进PARP2-DNA捕获的小分子
传统的PARP酶活性抑制试验仅能反映化合物对催化活性的抑制,无法区分“催化抑制”与“DNA捕获”两种机制。而PARPtrap试剂盒直接检测PARP2-DNA复合物的稳定性,可精准识别能够增强而非破坏该复合物的化合物。这对于开发具有更强细胞毒性效应的下一代PARP抑制剂(如PARP2选择性捕获剂)至关重要。试剂盒兼容自动化移液工作站,384孔板格式支持每天数千个化合物的筛选。
2. 先导化合物的IC₅₀测定及机制表征
对于筛选出的阳性化合物,可进一步进行剂量-响应曲线分析,计算其促进PARP2-DNA捕获的半效浓度(EC₅₀)或IC₅₀。由于荧光偏振读数稳定、Z'因子高,该方法能够可靠区分不同化合物之间的效力差异。研究者还可以通过改变NAD⁺浓度或DNA序列,探究化合物的作用模式(如是否与DNA结合位点竞争)。
四、实验流程简要说明
1. 试剂准备:将PARP2酶、荧光DNA探针、NAD⁺及检测缓冲液置于冰上解冻,避光保存荧光探针。准备待测化合物(建议使用DMSO溶解,并设置浓度梯度)。
2. 反应体系构建(384孔板推荐方案):每孔加入10 uL检测缓冲液,随后加入2 uL PARP2酶(终浓度优化范围为10–100 nM),2 uL荧光DNA探针(终浓度5–20 nM),2 uL NAD⁺(终浓度100 uM),以及2 uL待测化合物或DMSO对照。总体积调整至20 uL。
3. 孵育与读数:室温避光孵育30–60分钟。使用荧光偏振酶标仪,激发波长485 nm,发射波长535 nm,分别测量平行偏振(S)和垂直偏振(P)信号,计算偏振值mP = 1000 × (S - G×P)/(S + G×P),其中G为仪器校正因子。
4. 数据分析:将化合物孔的mP值与阴性对照(无化合物,PARP2正常解离)及阳性对照(使用已知捕获型抑制剂,如奥拉帕尼或特定PARP2工具化合物)进行比较。捕获活性% = (mP_compound - mP_min) / (mP_max - mP_min) × 100%,绘制剂量-响应曲线拟合EC50。
五、注意事项与配套建议
物种特异性:试剂盒提供人源PARP2重组蛋白,其DNA结合域与啮齿类动物同源性较高,但跨物种验证需用户自行评估。
阳性对照:首次使用建议运行已知的PARP捕获剂(如talazoparib,虽主要靶向PARP1但对PARP2也有一定捕获效应),以确认体系性能。
背景控制:无PARP2酶的孔作为空白对照,测定荧光探针的基础偏振值。NAD⁺缺失的孔可反映最大结合信号(因无自身修饰解离)。
辅助设备:需要具备荧光偏振检测模块的多模式酶标仪,以及黑色、低自发荧光的384孔板。
干扰排除:某些化合物自身可能具有荧光或淬灭效应,建议设置“化合物+荧光探针(无酶)”对照孔,排除假阳性。
六、文献参考
Murai J., et al., 2014 Molecular Cancer Therapeutics 13: 433-443
Murai J., et. al., 2012 Cancer Research 72: 5588-5599
Zandarashvili L., et al., 2020 Science 368(6486): 6367
Marques M., et al., 2019 Oncogene 38 (12): 2177-2191.
DR3:TL1A抑制剂筛选检测试剂盒:化学发光检测,支持HTS及抗体药物表征
在肿瘤免疫治疗领域,靶向共刺激或共抑制受体已成为突破性策略。DR3(死亡受体3,也称TNFRSF25)作为TNF受体超家族成员,主要在T细胞和NK细胞上表达。其配体TL1A(TNFSF15)则表达于单核细胞、巨噬细胞、树突状细胞及部分非免疫细胞。DR3与TL1A结合后,可调节效应细胞的增殖、活化、凋亡及趋化因子产生,在T细胞介导的免疫应答中发挥关键作用。近年研究表明,抑制DR3-TL1A相互作用在实体瘤治疗中具有显著的治疗潜力。因此,开发能够阻断这一蛋白-蛋白相互作用的抑制剂(小分子或生物制剂)成为药物发现的热点方向。
由艾美捷代理BPS Bioscience推出的DR3:TL1A Inhibitor Screening Assay Kit(货号:82241),正是为高通量筛选和表征DR3-TL1A相互作用抑制剂而设计的完整化学发光检测方案。该试剂盒采用基于ELISA原理的竞争性或直接结合检测模式,以96孔或384孔板形式运行,可快速评估化合物或抗体对DR3与TL1A结合的阻断效果。以下从检测原理、试剂盒组分、操作流程及应用场景等方面进行详细介绍。
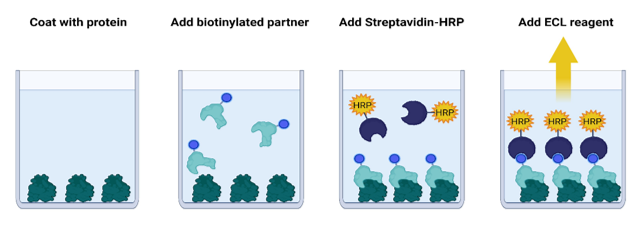
图1:DR3:TL1A抑制剂筛选检测试剂盒工作流程图。
首先,将DR3涂覆在96孔板或384孔板上。接下来,将生物素化的TL1A与DR3一起孵育。最后,用链霉亲和素-辣根过氧化物酶(HRP)处理板,然后加入HRP底物以产生化学发光。化学发光信号与DR3:TL1A的结合成比例
一、检测原理:固相结合-化学发光读出
本试剂盒采用固相蛋白-蛋白相互作用检测模式,核心流程如下:
1. 配体包被:利用试剂盒提供的生物素标记TL1A蛋白(biotin-labeled TL1A,氨基酸72至C端),通过生物素-链霉亲和素相互作用将其固定在预先包被链霉亲和素的微孔板上。这一固定化过程保持了TL1A的天然构象和结合活性。
2. 受体结合:加入纯化的DR3蛋白(氨基酸25-199,即胞外结构域),在优化缓冲液中与固定的TL1A发生特异性结合。若体系中存在抑制剂(小分子或抗体),则会竞争性或变构性地阻断DR3与TL1A的相互作用,导致结合到板上的DR3量减少。
3. 信号检测:洗涤去除未结合的DR3后,加入链霉亲和素标记的辣根过氧化物酶(streptavidin-labeled HRP)。该酶通过链霉亲和素与生物素化TL1A结合(不依赖DR3),因此信号强度理论上应与TL1A的包被量成正比。但为了检测DR3的结合量,实际试剂盒中还需依赖额外的检测抗体。根据BPS Bioscience同类产品设计惯例,该试剂盒包含抗DR3的一抗及HRP标记的二抗,或直接使用HRP标记的抗DR3抗体。用户手册会提供详细步骤。最终加入化学发光底物,HRP催化产生光信号,光强度与结合在板上的DR3量呈正相关。
4. 数据解读:抑制剂存在时,DR3结合减少,光信号降低;无抑制剂时信号最高。通过计算抑制率来评价化合物的阻断效力。
二、试剂盒组分与规格
该试剂盒提供两种规格:96孔板形式(100次反应)和384孔板形式(400次反应),每个试剂盒包含以下核心组分:
生物素标记的TL1A(biotin-labeled TL1A,氨基酸72至C端)
纯化的人源DR3蛋白(氨基酸25-199)
链霉亲和素标记的HRP(streptavidin-labeled HRP)
检测缓冲液(经优化以维持蛋白稳定性和结合特异性)
详细操作说明书
此外,试剂盒中通常包含链霉亲和素预包被的微孔板(未明确写出,但根据“convenient 96-well or 384-well format”及同类产品惯例,板条已包含在内)。所有组分在收货后按指示存储(建议-80°C),自收货之日起6个月内保持最佳性能。
三、应用场景
本试剂盒主要面向两大药物发现需求:
1. 小分子抑制剂或生物制剂的筛选
在药物发现早期,研究者可使用该试剂盒对化合物库或抗体文库进行高通量筛选(HTS),快速识别能够阻断DR3-TL1A相互作用的候选分子。384孔板格式支持自动化工作站,每天可完成数千个样品的初筛。检测体系为均相(结合后洗涤),化学发光信号稳定,Z'因子通常大于0.7,适合高置信度筛选。
2. 抑制剂的滴定与IC50测定
对于初筛获得的阳性化合物,可进一步进行剂量-响应曲线分析。将待测样品稀释为8-12个浓度梯度,按相同流程检测,计算每个浓度的抑制率,使用四参数逻辑回归拟合IC₅₀值。该方法同样适用于抗体药物的亲和力排序及表位竞争分析。
四、实验流程简要说明
以下为典型96孔板操作流程:
1. 试剂准备:将所有组分从-80°C取出,置于冰上解冻。平衡检测缓冲液至室温。准备待测抑制剂稀释系列(建议使用检测缓冲液稀释,保持DMSO终浓度≤1%)。
2. 包被:将生物素标记的TL1A用检测缓冲液稀释至推荐浓度(如0.5-2 ug/mL),每孔加入50 uL,用封板膜覆盖,4°C过夜或室温孵育2小时。或者使用预包被链霉亲和素的板,直接加入生物素-TL1A室温孵育1小时。
3. 洗涤:弃去包被液,每孔加入200 uL PBST,洗涤3次,每次振荡30秒后弃去。
4. 抑制剂与DR3共孵育:每孔加入25 uL检测缓冲液,然后加入25 uL稀释的待测化合物(或对照孔加入缓冲液/已知抑制剂),最后加入25 uL DR3蛋白(终浓度需预实验优化)。室温振荡孵育1-2小时。
5. 检测:洗涤3次后,加入链霉亲和素-HRP(及抗DR3检测抗体,按试剂盒说明稀释),室温孵育30-60分钟。再次洗涤后,加入化学发光底物,立即在酶标仪上读取发光值(积分时间100-500毫秒)。
6. 数据分析:计算抑制率% = (信号_max - 信号_sample) / (信号_max - 信号_min) × 100%,其中信号_max为无抑制剂对照孔,信号_min为无DR3或无TL1A的背景对照孔。使用GraphPad等软件拟合IC₅₀。
五、存储稳定性
该试剂盒所有组分在收货后按指示温度(通常为-80°C)储存,自收货之日起6个月内性能稳定。荧光标记物(如有)需避光保存。建议将生物素-TL1A和DR3蛋白分装为单次使用量,避免反复冻融导致活性下降。
六、文献参考
Xu, W. D., et al., 2022 Front. Immunol. 13: 1-10.
Zwolak, A., et al., 2022 Sci. Rep. 12(1): 20538.
FAP荧光检测试剂盒:酶动力学与药物发现实时检测方案
在肿瘤微环境研究中,成纤维细胞活化蛋白(Fibroblast Activation Protein, FAP)正成为一个备受关注的治疗靶点。FAP是一种II型跨膜丝氨酸蛋白酶,属于二肽基肽酶(DPP)亚家族,在正常成人组织中表达极低,但在多种实体瘤(包括乳腺癌、肺癌、前列腺癌、胰腺癌和宫颈癌)的癌相关成纤维细胞(CAF)表面显著上调。FAP通过切割PEDF、血管生成素-1和VEGF-C等基质蛋白,同时上调TGF-β,从而塑造免疫抑制性微环境,促进肿瘤侵袭和转移。研究表明,敲除FAP可减少胰腺导管腺癌的转移。此外,FAP独特的表达谱使其成为小分子抑制剂和CAR-T细胞疗法的理想靶点,多项临床前及临床试验正在进行中。因此,开发能够高效检测FAP蛋白酶活性并筛选其抑制剂的工具,对于抗肿瘤药物发现至关重要。
由艾美捷代理的BPS Bioscience推出的FAP Fluorogenic Assay Kit(货号:80210),正是为满足上述需求而设计的一套完整荧光检测解决方案。该试剂盒采用荧光底物法,可快速、灵敏地定量FAP的蛋白酶活性,适用于酶动力学研究、小分子抑制剂筛选及高通量筛选(HTS)。以下从检测原理、试剂盒组分、操作流程、应用场景及性能特点等方面进行详细介绍。
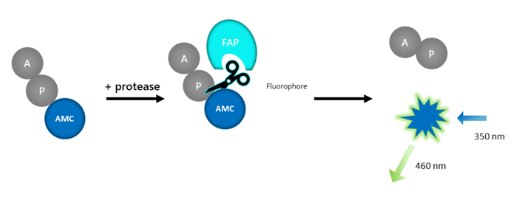
图1:测定原理示意图。
荧光DPP底物1是一种荧光肽底物(Ala-Pro-AMC二肽)。在共轭形式下,荧光染料AMC发出的能量被猝灭。蛋白水解作用会释放AMC并发出荧光。荧光的增加与FAP活性直接成正比。
一、检测原理:荧光底物法实时监测蛋白酶活性
本试剂盒的核心检测原理基于荧光共振能量转移(FRET)或直接荧光释放机制:
荧光底物:试剂盒提供一种针对DPP家族(尤其是FAP)优化的荧光底物。该底物由一个短肽序列(通常为Z-Gly-Pro-AMC或类似结构)共价连接荧光基团(如7-氨基-4-甲基香豆素,AMC)组成。在天然状态下,肽段与荧光基团的连接导致荧光淬灭或发射波长偏移。
酶切反应:当加入含有FAP的样品后,FAP特异性切割肽段中脯氨酸之后的酰胺键,释放出游离的荧光基团AMC。
荧光检测:游离AMC在激发波长约380 nm、发射波长约460 nm处产生强烈的荧光信号。荧光强度随时间线性增加,其速率(RFU/min)直接反映FAP的蛋白酶活性。
抑制剂评估:若体系中加入FAP抑制剂,酶活性被抑制,荧光生成速率下降。通过对比抑制剂组与对照组(DMSO或无抑制剂)的初始速率,计算抑制率及IC₅₀。
这一检测模式具有以下技术优势:均相(无需分离步骤)、实时(可动态监测反应进程)、高灵敏度(检测下限可达纳摩尔级)以及高通量兼容(96孔板格式适配自动化酶标仪)。
二、试剂盒组分与规格
该试剂盒为96孔板格式,包含足够进行100次酶反应的全部核心组分:
重组人FAP酶(氨基酸29-760):包含完整的胞外催化结构域,经纯化及活性验证,确保批次间一致性。
DPP荧光底物:即用型溶液,对光敏感,需避光保存。
DPP检测缓冲液:经优化的pH及离子强度,维持FAP的最佳催化活性。
详细操作说明书:包含推荐的反应体系、酶稀释方案及数据分析方法。
所有组分在收货后按指示存储(建议-80°C),自收货之日起6个月内保持最佳性能。荧光底物应避免反复冻融及长时间光照,建议分装后于-20°C避光保存。
三、应用场景
本试剂盒主要面向以下三类核心应用:
1. 小分子抑制剂的筛选与IC50测定
在抗肿瘤药物发现项目中,研究者可使用该试剂盒对化合物库进行高通量筛选,快速识别具有FAP抑制活性的先导化合物。由于检测体系简单、成本适中,适合作为初筛方法。对于阳性化合物,可进一步进行剂量-响应曲线分析,获得IC₅₀值,用于构效关系研究。
2. 酶动力学研究
通过改变底物浓度(固定酶量)测定不同条件下的反应速率,可计算FAP的米氏常数和最大反应速率。同样,改变酶浓度可验证线性范围。这些参数对于理解FAP的催化机制及不同突变体的功能差异具有重要意义。
3. 抗体或生物制剂的阻断活性评价
除小分子外,该试剂盒也可用于评估抗FAP抗体或基于蛋白质的抑制剂是否能够阻断FAP的蛋白酶活性。只需将抗体与FAP预孵育,然后按标准流程加入底物即可。
四、性能特点与注意事项
线性范围:在优化的酶浓度(如1 nM FAP)和底物浓度下,反应可在30–60分钟内保持线性,确保速率计算的准确性。
Z'因子:在384孔板格式(若用户自行转换)下,该检测体系通常Z' > 0.6,适合高通量筛选。
背景控制:设置无酶对照孔以扣除底物自发水解产生的背景荧光。同时建议设置无底物对照,评估样品自身荧光。
抑制剂干扰排除:某些化合物可能在380/460 nm处有自发荧光或吸收,导致假阳性/假阴性。建议设置“抑制剂+底物(无酶)”对照,并在数据分析时进行校正。
底物特异性:该试剂盒使用的DPP底物可被FAP以及同家族成员DPP4、DPP8、DPP9等切割。若需验证抑制剂的FAP选择性,建议使用重组单一酶进行平行比较。
五、存储稳定性与运输条件
试剂盒采用-80°C干冰运输。收货后,FAP酶和荧光底物应立即存放于-80°C,检测缓冲液可于-20°C或4°C短期保存(以说明书为准)。避免反复冻融:建议将酶分装为单次使用量(例如10 uL/管),底物按需分装。在正确存储条件下,所有组分自收货之日起6个月内性能稳定。
六、文献参考
Pure E. and Blomberg R., 2018, Oncogene 37: 4343-4357.
Bughda R., et al., 2021, Immunotargets Ther. 10:313-323.
Keap1:Nrf2抑制剂筛选检测试剂盒:高通量抗氧化通路调节剂筛选工具
氧化应激与炎症反应是多种慢性疾病(包括神经退行性疾病、心血管疾病、糖尿病及癌症)的核心病理机制之一。在细胞对抗氧化应激的过程中,转录因子Nrf2(核因子红细胞2相关因子2)发挥着关键的“主调节器”作用。正常情况下,Nrf2在细胞质中被Keap1(Kelch样ECH关联蛋白1)结合并锚定,Keap1作为E3泛素连接酶复合物的底物识别亚基,持续介导Nrf2的泛素化降解,使其维持在较低水平。当细胞暴露于氧化应激或亲电试剂时,Keap1的关键半胱氨酸残基被修饰,构象发生变化,导致Nrf2从Keap1上释放并转位进入细胞核。入核后的Nrf2与ARE(抗氧化反应元件)结合,启动一系列抗氧化蛋白和II相解毒酶(如HO-1、NQO1、GCLC等)的表达,从而保护细胞免受氧化损伤。
鉴于Nrf2/Keap1信号轴在细胞保护中的核心地位,该通路已成为药物发现的明星靶点。激活Nrf2(通过破坏Keap1-Nrf2相互作用)可用于治疗以氧化应激为特征的疾病,如慢性肾病、慢性阻塞性肺病、多发性硬化症等;而在某些癌细胞中,Nrf2的持续激活则促进肿瘤存活和化疗耐药,此时恢复Keap1功能或抑制Nrf2则成为治疗策略。因此,筛选能够阻断Keap1与Nrf2结合的小分子抑制剂,对于开发新型抗氧化药物或辅助化疗增敏剂均具有重要意义。
由艾美捷代理BPS Bioscience推出的Keap1:Nrf2 Inhibitor Screening Assay Kit(货号:72020),正是为满足上述需求而设计的一套完整荧光偏振(Fluorescence Polarization, FP)检测方案。该试剂盒采用96孔板格式,通过监测荧光标记Nrf2肽段与Keap1蛋白结合后旋转运动性的变化,快速、定量地评估化合物对Keap1:Nrf2相互作用的阻断能力,适用于高通量筛选及IC₅₀测定。以下从检测原理、试剂盒组分、操作流程、应用场景及性能特点等方面进行详细介绍。
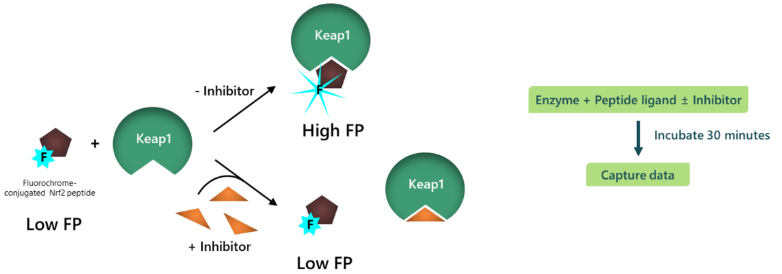
图1. Keap1:Nrf2抑制剂筛选检测试剂盒示意图。
一、检测原理:荧光偏振法监测蛋白-肽段相互作用
荧光偏振是一种基于分子旋转运动性变化来研究分子间相互作用的经典技术,具有均相、无需分离、实时检测等突出优势。其核心原理如下:
当一个小分子荧光团(如荧光素)被偏振光激发时,发射光的偏振程度与其在激发态寿命内的旋转速度密切相关。小分子物质(如自由的荧光标记肽段)旋转速度快,发射光偏振度低;而大分子复合物(如荧光肽段与较大的Keap1蛋白结合后)旋转速度显著减慢,发射光偏振度升高。偏振值通常以毫偏单位(mP)表示。
在本试剂盒中:
荧光标记的Nrf2肽段:该肽段包含Nrf2与Keap1结合所必需的核心基序——ETGE基序,其C端或N端共价连接荧光基团(如FAM)。该肽段分子量较小(约2–3 kDa),自由状态时偏振值较低。
Keap1蛋白:重组人源Keap1蛋白(包含其Kelch结构域,该结构域负责识别Nrf2的ETGE基序)。Keap1分子量约为70 kDa(全长)或Kelch结构域约35 kDa,远大于荧光肽段。
结合反应:当荧光Nrf2肽段与Keap1蛋白结合后,形成分子量约为肽段+Keap1的复合物,旋转速度下降,荧光偏振值显著升高(通常从约50 mP上升至150–200 mP)。
抑制剂效应:若待测化合物能够阻断Keap1与Nrf2肽段的相互作用,则荧光肽段无法被Keap1捕获,保持自由状态,偏振值维持在较低水平。通过比较加抑制剂前后偏振值的变化,即可计算抑制率。
这一检测模式直接评估化合物对蛋白-蛋白相互作用的破坏能力,而非间接测量下游功能变化,因此具有高特异性、高灵敏度及良好的可重复性,非常适合作为先导化合物筛选的主要方法。
二、试剂盒组分与规格
该试剂盒为96孔板格式,包含足够进行100次结合反应的全部核心组分:
纯化的Keap1蛋白:重组人源Keap1,通常为全长或包含Kelch结构域的活性片段,经质控验证具有Nrf2肽段结合活性。
荧光标记的Nrf2肽段:包含ETGE基序,荧光基团为FAM(激发/发射约485/535 nm),避光保存。
检测缓冲液:经优化的缓冲体系(含适当盐浓度、pH稳定剂及去垢剂),以维持蛋白稳定性并降低非特异性结合。
详细操作说明书:包含蛋白和肽段的推荐工作浓度、稀释方法及数据分析模板。
所有组分在收货后按指示存储(通常为-80°C),自收货之日起6个月内保持最佳性能。荧光肽段对光敏感,需避光保存并避免反复冻融。
三、实验流程简要说明
以下为典型96孔板单次反应的操作步骤(半面积板或常规板均可):
1. 试剂准备
从-80°C取出Keap1蛋白、荧光Nrf2肽段和检测缓冲液,置于冰上解冻。
平衡检测缓冲液至室温。荧光肽段解冻后短暂离心,置于冰上避光保存。
准备待测抑制剂:用DMSO或检测缓冲液稀释至所需浓度(建议设置10个浓度梯度,3倍或2倍倍比稀释)。
2. 反应体系构建(每孔总体积50–100 μL,以说明书为准)
加入检测缓冲液补足体积。
加入荧光Nrf2肽段至终浓度(通常为5–20 nM)。
加入待测抑制剂或对照(空白对照为缓冲液,阴性对照为DMSO,阳性对照可使用已知Keap1-Nrf2抑制剂如ML385或KI696等,但需用户自备)。
加入Keap1蛋白至终浓度(通常为50–200 nM,需预实验确定EC₈₀浓度)。
推荐先混合肽段和抑制剂,最后加入Keap1启动反应。
3. 孵育与读数
用封板膜覆盖96孔板,室温避光孵育30–60分钟,使反应达到平衡。
使用具备荧光偏振检测模块的酶标仪,设定激发波长485 nm,发射波长535 nm。分别读取平行偏振(S)和垂直偏振(P)信号。
计算每孔的偏振值(mP):
四、存储稳定性与运输条件
试剂盒采用-80°C干冰运输。收货后,Keap1蛋白和荧光肽段应立即存放于-80°C,检测缓冲液可于-20°C或4°C短期保存。荧光肽段需严格避光。建议将蛋白和肽段分装为单次使用量,避免反复冻融。在正确存储条件下,所有组分自收货之日起6个月内性能稳定。
五、文献参考
Inoyama, D., et al. 2012. J. Biomol. Screening 17(4): 435-447
CDK9/CyclinT激酶检测试剂盒:支持IC50测定及酶动力学研究
在肿瘤生物学研究中,转录失调是驱动癌细胞增殖和耐药的关键机制之一。CDK9(周期蛋白依赖性激酶9)作为正性转录延伸因子b(P-TEFb)复合物的催化亚基,与周期蛋白CyclinT共同调控RNA聚合酶II的C端结构域磷酸化,从而控制基因转录延伸过程。多种癌基因(如MYC、雄激素受体AR等)的转录高度依赖CDK9-CyclinT复合物的活性。CDK9的过度活化与肿瘤发生及治疗耐药密切相关,因此靶向CDK9-CyclinT已成为抗癌药物开发的热点方向。近年来,除了传统小分子抑制剂,靶向蛋白降解(PROTAC)技术也取得了突破——例如选择性CDK9-CyclinT降解剂LL-K9-3在22RV1细胞中显示出比亲本抑制剂SNS032及PROTAC分子Thal-SNS032更强的降AR和cMyc效果。这些进展凸显了可靠、高效的CDK9激酶活性检测方法在药物发现中的重要性。
艾美捷代理BPS Bioscience推出的CDK9/CyclinT Kinase Assay Kit(货号:79628),正是为满足激酶抑制剂筛选和酶动力学研究需求而设计的一套完整发光法检测方案。该试剂盒采用Kinase-Glo Max作为检测试剂,通过定量反应后剩余ATP的含量来反映激酶活性,具有操作简便、灵敏度高、动态范围宽及高通量兼容等突出优势。以下从检测原理、试剂盒组分、操作流程、应用场景及性能特点等方面进行详细介绍。
一、检测原理:基于ATP消耗的发光法定量激酶活性
本试剂盒的核心检测原理为“激酶反应-剩余ATP检测”偶联法:
激酶反应:在含有重组人源CDK9/CyclinT复合物、特定激酶底物(如组蛋白或合成肽段)及ATP的反应体系中,CDK9/CyclinT催化底物磷酸化,同时将ATP转化为ADP。反应过程中ATP被持续消耗。
终止与检测:反应进行一定时间后,加入Kinase-Glo Max发光试剂。该试剂含有热稳定性荧光素酶及其底物荧光素。当体系中存在剩余ATP时,荧光素酶催化荧光素氧化产生稳定发光信号。发光强度与ATP剩余量呈正比,与激酶活性呈反比。
信号转换:在无激酶或激酶被完全抑制的情况下,ATP消耗最少,发光信号最高;反之,激酶活性越强,ATP消耗越多,发光信号越低。通过比较待测样品孔与对照孔的发光值,即可计算激酶活性或抑制率。
这一检测模式具有以下技术优势:均相(无需分离磷酸化产物)、高灵敏度(检测低至亚微摩尔ATP)、宽动态范围(超过4个数量级)以及操作简便(仅需“混合-孵育-读数”三步)。与传统放射性同位素法(如³²P-ATP掺入)相比,避免了放射性危害和废料处理问题;与荧光法相比,无需激发光源,不受化合物自发荧光干扰。
二、试剂盒组分与规格
该试剂盒提供两种规格:96孔板形式(100次反应)和384孔板形式(400次反应),每个试剂盒包含以下核心组分:
重组人CDK9/CyclinT激酶:纯化的活性复合物,经质控验证具有底物磷酸化活性。
激酶底物:适用于CDK9的底物,通常为含有特定丝氨酸/苏氨酸残基的合成肽段或全长蛋白。
ATP:高纯度三磷酸腺苷,浓度经标定。
激酶检测缓冲液:优化pH及离子成分,维持激酶最佳活性。
Kinase-Glo Max 发光试剂:即用型,避光保存。
详细操作说明书:包含推荐反应体系、孵育时间及数据分析方法。
所有组分在收货后按指示存储(通常为-80°C),自收货之日起6个月内保持最佳性能。Kinase-Glo试剂需避免反复冻融,建议分装后于-20°C避光保存。
三、实验流程简要说明
以下为典型96孔板单次反应的操作步骤(总体积50 uL):
1. 试剂准备
从-80°C取出CDK9/CyclinT激酶、底物、ATP及检测缓冲液,置于冰上解冻。
平衡检测缓冲液至室温。Kinase-Glo试剂提前30分钟取出平衡至室温(避免反复加热)。
准备待测抑制剂:用DMSO或缓冲液稀释至所需浓度(建议设置10个浓度梯度,2倍或3倍倍比稀释)。注意最终DMSO浓度不得超过1%(详见禁忌说明)。
2. 激酶反应体系构建
每孔加入10 uL检测缓冲液。
加入2 uL待测抑制剂或对照(DMSO/缓冲液/阳性对照如SNS032或LL-K9-3)。
加入5 uL CDK9/CyclinT激酶(推荐起始浓度0.5–10 nM,需预实验优化至消耗30–50% ATP)。
加入10 uL激酶底物(终浓度依说明书推荐,通常为0.1–1 ug/孔)。
加入3 uL ATP(终浓度通常为10–100 uM,接近或低于Kₘ值以获得最佳抑制灵敏度)。
用检测缓冲液补足总体积至25 uL(具体体积以说明书为准)。启动反应。
3. 激酶反应孵育
用封板膜覆盖,室温或30°C孵育30–60分钟(使ATP消耗处于线性区间)。
4. 发光检测
加入25 uL Kinase-Glo Max试剂(与反应体系等体积)。
在摇床上混合1–2分钟,室温孵育10–30分钟(使发光信号稳定)。
使用发光酶标仪(读板模式:终点法,积分时间0.5–1秒)读取发光值(RLU)。
5. 数据分析
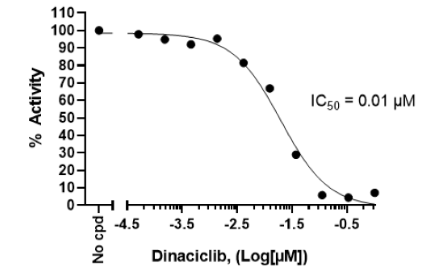
Dinaciclib抑制CDK9/CyclinT激酶活性。
四、应用场景
本试剂盒主要面向以下两大类核心应用:
1. 小分子激酶抑制剂的筛选与IC50测定
2. 酶动力学研究
五、性能特点与注意事项
线性范围与Z'因子:在优化条件下(激酶消耗30–50% ATP),Z'因子通常大于0.7,满足高通量筛选对统计学可靠性的要求。信号窗口(信背比)通常>5倍。
DMSO耐受性:体系中DMSO终浓度不得超过1%(见Contraindications),否则会抑制激酶活性或干扰荧光素酶反应。建议将化合物母液浓度配制成至少100×,加入反应体系后稀释至1%以下。
ATP浓度选择:为筛选ATP竞争性抑制剂,建议使用接近或低于Kₘ的ATP浓度(如10 uM);为评估非竞争性抑制剂或进行选择性谱分析,可使用饱和ATP浓度(如1 mM)。用户需根据研究目的调整。
反应时间优化:首次使用应进行时间进程实验,确保激酶反应在线性区间内(通常30–60分钟)。过度反应导致ATP耗尽,将无法区分抑制程度的差异。
阳性对照:建议使用已知CDK9抑制剂如SNS032、 flavopiridol或降解剂LL-K9-3作为阳性对照,验证体系性能。
化合物干扰排除:某些化合物可能抑制荧光素酶活性(“火萤光素酶抑制剂”)或淬灭发光信号。建议设置“化合物+Kinase-Glo(无激酶反应体系)”对照,评估化合物对检测试剂的直接影响。若存在干扰,需使用替代检测方法(如放射性滤膜结合法)进行交叉验证。
六、文献参考
Napolitano G, et al., 2003 J Cell Physiol. 197(1):1-7.
Li J., et al., 2022 J Med Chem. 65(16):11034-11057.
PARP2化学发光检测试剂盒:信噪比优异,适用于化合物库筛选
在DNA损伤修复领域,PARP家族是一类关键的核酶,通过催化多聚ADP-核糖化(PARylation)参与DNA单链断裂修复、基因组稳定性维持及细胞应激响应。PARP2作为该家族的重要成员,虽然仅贡献约10%的总PARP活性,但在DNA修复、氧化应激应答及线粒体片段化中发挥不可替代的作用。基因敲除研究显示,PARP2还参与脂肪生成、精子发生及胸腺细胞存活,并作为雌激素受体(ER)和过氧化物酶体增殖物激活受体(PPAR)的共调节因子。值得注意的是,PARP2在前列腺癌中过表达,并通过FOXA1/AR通路促进疾病进展。临床上已获批的PARP抑制剂(如奥拉帕尼、尼拉帕尼等)同时靶向PARP1和PARP2,但其对PARP2选择性抑制的贡献及潜在的治疗优势仍在深入研究中。因此,开发能够精准、高效检测PARP2酶活性的分析工具,对于靶向PARP2的药物发现及机制研究至关重要。
由艾美捷代理的BPS Bioscience推出的PARP2 Chemiluminescent Assay Kit(货号:80552),正是为满足上述需求而设计的一套完整化学发光检测方案。该试剂盒采用基于组蛋白包被板的ELISA原理,通过检测生物素化ADP-核糖掺入底物的量来定量PARP2的酶活性,适用于小分子抑制剂筛选、酶动力学研究及高通量筛选(HTS)。以下从检测原理、试剂盒组分、操作流程、应用场景及性能特点等方面进行详细介绍。
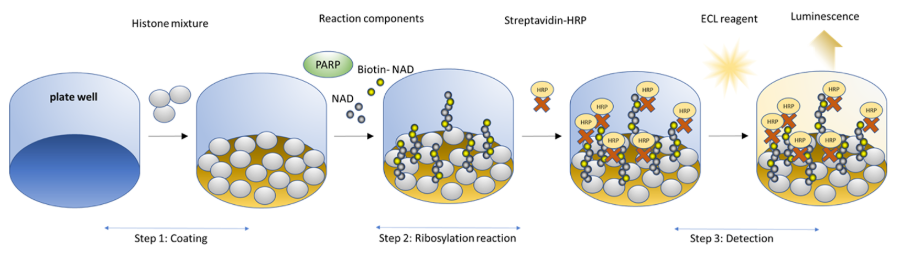
图1. PARP2化学发光检测试剂盒示意图。
组蛋白被涂覆在384孔板上。接下来,在优化的检测缓冲液中,将生物素化的NAD+混合物(称为PARP底物混合物)与PARP2酶和活化的DNA模板一起孵育。然后,用链霉亲和素-HRP处理板,随后加入ELISA ECL底物,产生化学发光,可使用化学发光仪进行测量。化学发光信号与PARP2活性成正比。
一、检测原理:化学发光法定量PARP2的自身PARylation及底物PARylation
本试剂盒采用经典的PARP酶活性ELISA检测模式,核心原理如下:
底物包被:96孔或384孔板预先包被组蛋白或特定核蛋白作为PARP2的底物。组蛋白是PARP家族天然底物,其上的谷氨酸残基可被PARylation修饰。
PARP2反应:加入重组人源PARP2酶(氨基酸2-583,包含催化结构域和DNA结合域)、生物素化NAD⁺(biotin-NAD⁺,作为ADP-核糖供体)以及含活化DNA的PARP检测缓冲液。在DNA存在下,PARP2被激活,催化生物素化ADP-核糖单元聚合到组蛋白底物上,同时发生自身PARylation。反应产物为生物素标记的PAR链。
检测:洗涤去除未结合的试剂后,加入链霉亲和素标记的辣根过氧化物酶(Streptavidin-HRP)。链霉亲和素与生物素化PAR链高效结合。再次洗涤后,加入化学发光HRP底物,HRP催化产生光信号。发光强度与固定化PAR链的量呈正比,即与PARP2酶活性呈正比。
抑制剂效应:若体系中加入PARP2抑制剂,酶活性被阻断,生物素化PAR链合成减少,发光信号降低。通过比较抑制剂组与对照组(DMSO或无抑制剂)的发光值,计算抑制率及IC50。
与荧光偏振法或荧光法相比,化学发光检测具有背景极低、信噪比高、动态范围宽的优势,尤其适合需要高灵敏度的筛选应用。同时,该方法为终点法(非实时),可批次处理大量样品,与自动化工作站兼容良好。
二、试剂盒组分与规格
该试剂盒提供两种规格:96孔板形式(100次反应)和384孔板形式(400次反应),每个试剂盒包含以下核心组分:
重组人PARP2酶(氨基酸2-583):纯化自昆虫细胞或大肠杆菌表达系统,经活性验证,确保批次间一致性。
生物素化NAD⁺(biotin-NAD⁺):即用型溶液,作为PARylation反应的ADP-核糖来源。
PARP检测缓冲液:含有活化DNA(如剪切的鲑鱼精DNA)及必要的辅因子(Mg²⁺、DTT等),以激活PARP2并维持其催化活性。
链霉亲和素-HRP:浓缩液,使用前需按说明书稀释。
化学发光底物:HRP的发光底物(如鲁米诺/过氧化物溶液)。
10×洗涤缓冲液:需稀释后使用。
封闭缓冲液:用于减少非特异性结合。
详细操作说明书:包含包被步骤、反应条件及数据分析模板。
所有组分在收货后按指示存储(通常为-80°C或-20°C,具体以说明书为准),自收货之日起6个月内保持最佳性能。生物素化NAD⁺和链霉亲和素-HRP需避免反复冻融。
三、实验流程简要说明
以下为典型96孔板操作流程(试剂盒通常已提供预包被组蛋白的板,或需用户自行包被,以说明书为准):
1. 试剂准备
从-80°C取出PARP2酶、生物素化NAD⁺、检测缓冲液等,置于冰上解冻。
准备待测抑制剂:用检测缓冲液或DMSO稀释至所需浓度(建议设置10个浓度梯度,2倍或3倍倍比稀释)。注意最终DMSO浓度不得超过1%(见禁忌说明)。
稀释洗涤缓冲液至1×工作浓度。
2. 反应体系构建
使用提供的预包被组蛋白微孔板(若未预包被,需先用组蛋白包被过夜,然后封闭)。
每孔加入50 uL检测缓冲液(含活化DNA)。
加入10 uL稀释的PARP2酶(推荐起始浓度0.5–5 nM,需预实验优化,使信号处于线性区间)。
加入10 uL待测抑制剂或对照(缓冲液/DMSO/阳性对照如奥拉帕尼、他拉唑帕尼等)。
室温预孵育10分钟。
加入10 uL生物素化NAD⁺(终浓度通常为0.5–2 uM)。
用封板膜覆盖,室温或30°C孵育30–60分钟(使PARylation反应充分进行)。
3. 检测步骤
弃去反应液,每孔加入200 uL 1×洗涤缓冲液,洗涤3次。
加入100 uL稀释的链霉亲和素-HRP(按说明书比例稀释),室温孵育30分钟。
再次洗涤3次。
加入100 uL化学发光底物,立即使用发光酶标仪读取发光值(RLU),积分时间0.5–1秒。
4. 数据分析
四、应用场景
本试剂盒主要面向以下两大类核心应用:
1. PARP2小分子抑制剂的筛选与IC50测定
2. 酶动力学研究与作用机制解析
五、存储稳定性与运输条件
试剂盒采用-80°C干冰运输。收货后,PARP2酶和生物素化NAD⁺应立即存放于-80°C;链霉亲和素-HRP和化学发光底物通常存放于-20°C(避光);检测缓冲液和洗涤缓冲液可于4°C保存。建议将PARP2酶分装为单次使用量(如2 uL/管),避免反复冻融。在正确存储条件下,所有组分自收货之日起6个月内性能稳定。
文献参考:
Gui B., et al., 2019 Proc Natl Acad Sci USA 116 (29): 14573-14582.
联系邮箱:kefu@labbase.net
版权与免责声明
- 凡本网注明“来源:来宝网”的所有作品,版权均属于来宝网,转载请必须注明来宝网, https://www.labbase.net,违反者本网将追究相关法律责任。
- 本网转载并注明自其它来源的作品,目的在于传递更多信息,并不代表本网赞同其观点或证实其内容的真实性,不承担此类作品侵权行为的直接责任及连带责任。其他媒体、网站或个人从本网转载时,必须保留本网注明的作品来源,并自负版权等法律责任。
- 如涉及作品内容、版权等问题,请在作品发表之日起一周内与本网联系,否则视为放弃相关权利。