细胞凋亡检测——细胞凋亡检测试剂盒解决方案
- http://www.abbkine.cn/apoptosis-detection-annexin-2021年3月16日 3:06 点击:868
其实从严格的词学意义上来说,细胞程序性死亡(PCD)与细胞凋亡是有很大区别的。细胞程序性死亡,是个功能性概念,描述在一个多细胞生物体中某些细胞死亡是个体发育中的一个预定的,并受到严格程序控制的正常组成部分。而细胞凋亡则是一个形态学的概念,描述一件有着一整套形态学特征的与坏死完全不同的细胞死亡形式。
细胞凋亡形态变化:细胞膜、细胞器相对完整,细胞核固缩
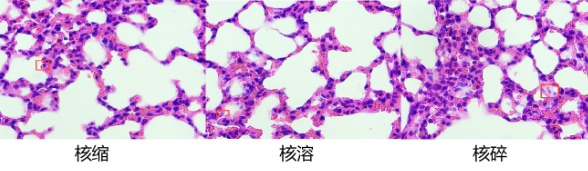
从左至右依次是细胞核核缩、核溶、核碎
接下来我们了解一下细胞凋亡的检——测——方——法:
按分类,细胞凋亡的检测方法有形态学检测、细胞功能检测,以及生化标记检测法。那么这些方法又有哪些优缺点呢?
1、形态学检测方法:
1)细胞器亚显微结构观察,电镜:
优点:凋亡检测金标准。
缺点:无法定量;实验步骤繁琐。
2)细胞核染色、镜检(Hoechst 33342)
优点:成本低、操作方便、可定量。
缺点:需对细胞进行计数。
2、细胞功能检测方法:
1)线粒体膜电位检测 JC-1,MitoTracker
优点:适合成像检测,染色结果只能用来判断线。
缺点:粒体膜电位是否丢失,不能定量。
2)细胞膜表面磷脂酰丝氨酸检测 Annexin V-AbFluor™ 488/PI
优点:受欢迎的细胞凋亡检测方法。
缺点:需制备单细胞悬液,可对凋亡不同时期比例进行定量。
3、生化标记检测法
1)凋亡分子标记检测 Caspase的活性检测 Caspase含量检测(WB)
优点:能够进行高通量筛选、可定量。
2)DNA损伤检测 DNA电泳 TUNEL法
优点:适合用于组织切片样本的凋亡研究。
缺点:电泳检测耗时,无法定量,稳定性差。
精准细胞凋亡检测的组合检测方法
一、Annexin V-AbFluor 488/PI检测方法
将Annexin V-AbFluor 488(绿色荧光)与PI(红色荧光)配合使用,可以准确的区分开凋亡早期、凋亡晚期及死细胞。
对于这种方法样本处理、染色操作及荧光的拍照决定了凋亡检测的精准度,对于不用样本及不同的检测方法,建议按照如下宝贵经验进行:
1、荧光拍照关键
1)悬浮细胞或重悬液制片拍照
将细胞用少量PBS或重悬液将细胞重悬成细胞浓缩液,吸取5-10ul在洁净的防脱载玻片上进行画圈涂片,盖上盖玻片立刻在显微镜下立即进行镜检。处理过程中注意速度,防止细胞死掉,重悬密度不易过小,进行涂片时以小于10ul的细胞悬液体积最适,整个操作建议在10min内完成。
2)细胞培养小皿或爬片拍照
皿底留有少量缓冲液,避免干片。拍照前一定先轻柔清洗,防止因清洗不充分导致拍照过程中有非特异性背景。
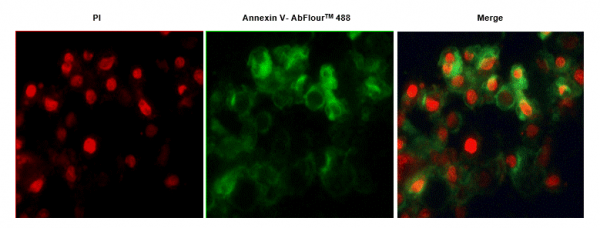
用喜树碱诱导Hela细胞24小时,用Annexin V-AbFluor 488凋亡检测试剂盒(KTA0002)进行染色。能被Annexin V- AbFluor 488/PI染色(绿色膜和红色碎片核)是早期凋亡细胞、坏死或晚期凋亡细胞。
2、流式实验关键步骤
1)消化细胞时避免假阳性
为防止假阳性的产生,消化细胞建议使用无EDTA的胰酶。
2)设置对照组
在流式细胞术中所测得的量是相对值,而非绝对值。如需知道绝对值则必
设置对照组,对照组包括有阴性对照和阳性对照。上机检测时建议设置空白组,Annexin V-AbFluor 488/PI单染组对照组,另需要提前调试好流式细胞仪。
3)检测的细胞量要适中
建议准备足量细胞,一般建议1×106 个细胞,如细胞太少检测时样本流量相对会增大从而影响变异系数,结果不准确,如细胞量太多加入的抗体或染料相对不足,结果也受影响。
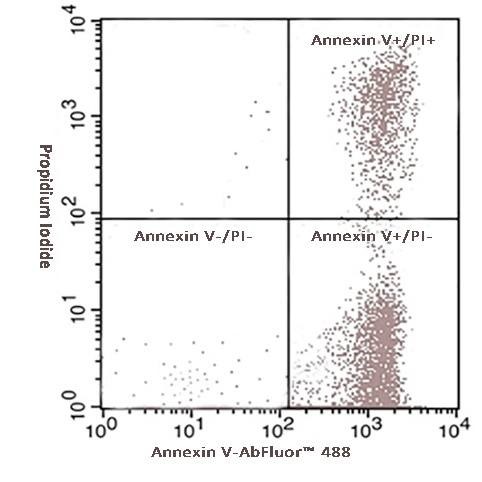
喜树碱诱导Hela细胞24小时,用Annexin V- AbFluor 488凋亡检测试剂盒(KTA0002,Abbkine)进行检测。使用Annexin V-AbFluor 488和碘化丙啶PI可以区分早期凋亡细胞(Annexin V- AbFluor™ 488阳性)、晚期凋亡或坏死细胞(Annexin V- AbFluor™ 488和碘化丙啶阳性)。
二、TUNEL检测方法
1、组织TUNEL实验中关键步骤
1)充分脱蜡和水化 <TIPS>
脱蜡前切片可以先在65℃烤箱中烘烤30min,再使用二甲苯进行脱蜡10-20min,而水化则用梯度乙醇从高浓度到低浓度浸洗5min。
2)把握好细胞通透的时间 <TIPS>
根据切片的厚薄选择蛋白酶k的孵育时间,蛋白酶K使用浓度不得低于
20 μg/mL,常用37℃处理10-30 min,6um切片时间稍短,20um切片增长时间,通过摸索达到既不脱片又能够使后面的酶和抗体进入胞内。处理时间过长易脱片、过短达不到通透效果。
3)适当延长TUNEL反应液时间 <TIPS>
建议处理条件是37℃反应2 h,可以根据预估的凋亡损伤程度选择更长的时间,建议结合最终的背景着色进行判断。
4)PBS的充分清洗 <TIPS>
在TUNEL反应后的清洗应十分严格,建议使用PBST重复清洗后再换PBS彻底清洗,或者增加PBS洗涤次数,因为这些清洗直接决定最后切片的非特异性着色。

小鼠肠道组织石蜡切片,200倍放大,红色荧光为发生晚期凋亡的细胞。
使用试剂:KTA2011 TUNEL法细胞凋亡检测试剂盒 (橙色荧光)、DAPI
操作步骤流程图:
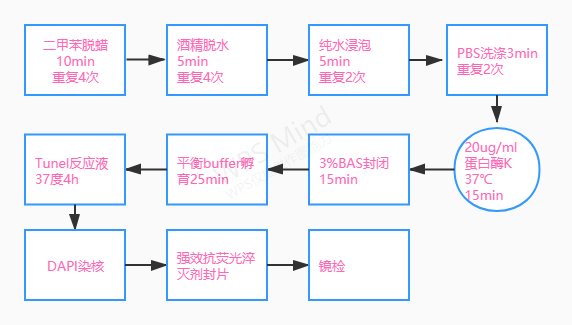
2、细胞TUNEL实验中关键步骤
1)加药模型的判断处理 <TIPS>
细胞样本做TUNEL时一定需要确认模型是否成功,在白光的镜检时需能明显判断凋亡的细胞。
2)蛋白酶k的使用<TIPS>
蛋白酶K目的是通透细胞膜和核膜,从而使反应试剂充分进入细胞核进行反应,提高阳性率。浓度过高或孵育时间太长非常容易使细胞脱落,建议使用20 μg/mL的蛋白酶K(0.5% Triton X-100),反应时间建议为5-15 min。
注意:关键试剂蛋白酶K一定需要摸索出最适合的使用条件。如温度过高,反应时间过长,易破坏核酸结构,出现假阳性。
文章来源:http://www.abbkine.cn/apoptosis-annexin-v-pi-tunel
————————————————————————————————
细胞增殖成像分析丨EdU细胞增殖检测试剂盒解决方案
细胞增殖的能力是评价细胞、代谢、生理、病理状况、细胞活性、基因毒性等的重要指标之一。
细胞增殖虽然与多种因素有关,比如细胞代谢活性、与细胞增殖相关的蛋白表达、ATP的浓度等等,但是检测细胞增殖现象的最直接最准确的方法就是用荧光探针直接检测遗传物质DNA的合成,这种方法是研究细胞增殖、信号通路、DNA修复及分化等等方向常用的方法。
目前,基于DNA的合成原理,人们最初开发了工具是BrdU染色法, 但是这种方法操作耗时长,往往需要过夜处理细胞,操作繁杂,比如需要DNA变性、抗原修复以及抗原抗体反应等操作,后来在BrdU的基础上,人们开发出了革命性的探针--EdU,这种方法不需要繁杂的操作,节约时间,且反应更灵敏和准确。并且与MTT/WST-1或者CCK-8这种依靠化学显色法只能得到一个折线图的方法相比,EdU 细胞增殖检测法可以得到高清细胞增殖现象数据图,可视化展示数据、更直观、更具视觉效果!
EdU的检测原理是什么?
EdU可以说是一款革命性的细胞增殖状态检测方法
与传统的免疫荧光染色(BrdU)检测方法相比, EdU只有BrdU抗体大小的1/500,在细胞内更容易扩散,不需要严格的样品变性(酸解、热解、酶解)处理,有效地避免了样品损伤,有助于在组织、器官的整体水平上观测细胞增殖的真实情况,具有更高的灵敏度和更快的检测速度。
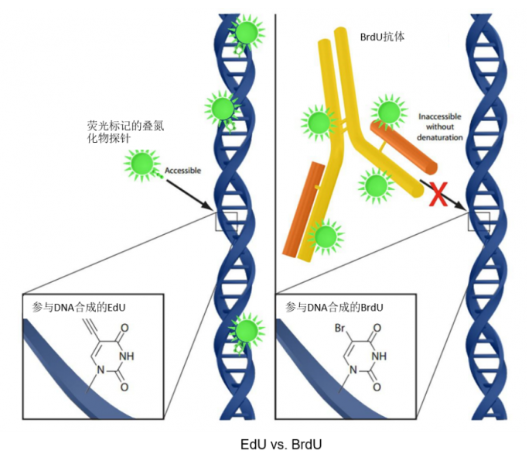
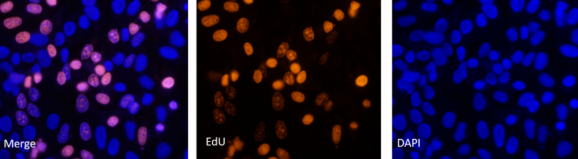
EdU细胞增殖检测法的操作教程
一、首先用 EdU 来标记细胞
注意:本实验样本是 Hela 细胞,如果使用其它类型的细胞,实验可能需要做调整。建议 EdU 起始浓度是 10 µM,或者根据细胞类型设置几个梯度预实验摸索最佳EdU浓度,再进行正式实验。
1.在六孔板里的盖玻片上培养细胞,使其生长至所需密度后处理细胞;
2.用 10 mM EdU 溶液在无血清培养基中制备 2x EdU 工作溶液;
3.预热 2x EdU 溶液,然后将 2x EdU 溶液添加到等体积含有实验细胞的培养基中,获得 1x EdU 溶液。例如,对于最终浓度为 10 µM 的溶液,可用 20 µM EdU 的新鲜培养基替换一半含细胞的培养基
注意:建议不要更换所有的培养基,因为这会影响细胞增殖速率;
将处理好的细胞孵育12小时;
孵育完成后立即进行步骤 B
二、细胞固定和透化
1.孵育后除去培养基,并向每个含有盖玻片的孔中加入2.5 mL含多聚甲醛的 PBS,室温下孵育15分钟;
2.除去固定液,用2.5 mL PBS洗涤孔中的细胞5分钟,重复三遍;
3.除去洗涤液,然后向前五个孔中加入2.5 mL通透液, 室温下孵育20分钟;
4.除去通透缓冲液,用2.5 mL PBS洗涤每个孔中的细胞两次,除去洗涤液;
5.立即进入步骤 C。
三、 EdU 检测
每孔使用 100 µL 反应混合物。反应混合物体积可根据实际情况进行调节,但必须按比例加入反应组分。
1.制备 Click-iT 反应混合物。注意要按表中列出的顺序添加成分,否则反应将无法得到最佳效果。配置好的 Click-iT 反应混合物必须在15分钟内使用。
2.向每个玻片上加入 100 µl Click-iT 反应混合物,室温下避光孵育 30 分钟;
3.除去反应混合物,用2.5 mL PBS洗涤每孔一次后,除去洗涤液;
可选择步骤:进行核染色(DAPI 或 Hoechst 33342)或抗体标记
提示:在孵育过程中一定要避光。如不需要其它染色,孵育后请直接进行成像和分析
Abbkine EdU细胞增殖检测试剂盒发表的文献:
1.Perilaldehyde activates AMP‐activated protein kinase to suppress the growth of gastric cancer via induction of autophagy
作者:Y Zhang, S Liu, Q Feng 杂志名称:JOURNAL OF CELLULAR BIOCHEMISTRY IF:3.09
2. In vitro mitochondrial-targeted antioxidant peptide induces apoptosis in cancer cells
作者:W Zhan, X Liao, L Li 杂志名称:Onco Targets Therv IF:2.31
文章来源:http://www.abbkine.cn/cell-proliferation-edu-image
——————————————————————————————
白介素-1β ELISA定量试剂盒:常见样本类型以及处理方法
ELISA常见的标本一般包括:液体类标本(包括血清、血浆、尿液、胸腹水、脑脊液、细胞培养上清等);培养细胞;组织标本。
那么是不是仅仅有了这些标本,就可以开始ELISA实验了呢?这些标本在收集的时间、方法以及保存条件都有一定的要求,划重点:
1.血清:全血样品于室温放置2小时或4℃过夜后于1000×g离心20分钟,取上清即可检测,收集血液的试管应为一次性的无热原、无内毒素试管。
2.血浆:抗凝剂推荐使用EDTA-2Na,样品采集后30分钟内于1000×g离心15分钟,取上清即可检测。避免使用溶血,高血脂样品。
3.组织匀浆:用预冷的匀浆液于5000×g离心5~10分钟,取上清检测。
4.细胞培养上清:取细胞培养上清于1000×g离心20分钟,除去杂质及细胞碎片。取上清检测。
5.其它生物样品:如固体生物代谢物,按组织样本处理方法操作,悬浮物应离心去除。
以上为样本的实验前处理方法,如果遇到急事不能立刻用这些新鲜的样本来进行实验的话,那么也无妨,接下来跟大家分享,样本处理后的储存方法,在短时间内是可以应急的,但是还是建议新鲜样本最佳:
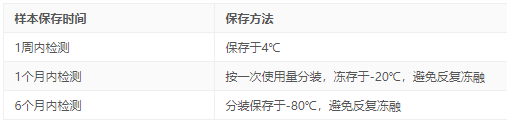
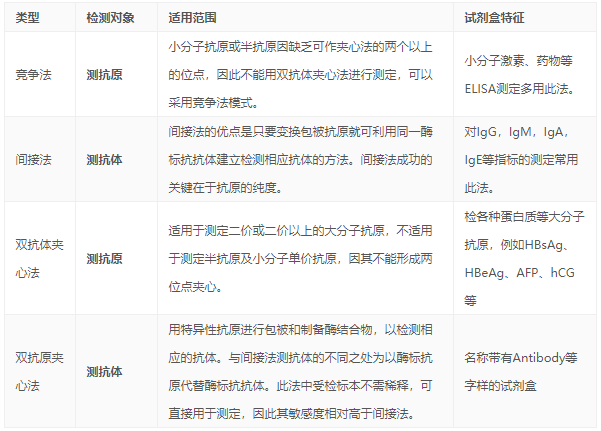
ELISA方法类型对比
一般ELISA实验类型有四种,竞争法、间接法、双抗体夹心法、双抗原夹心法,这四种方法有哪些不同,以及各自的优缺点是什么?
Abbkine白介素-1β ELISA定量试剂盒特点如下:
1、高效、灵敏、特异的抗体;
2、定量准确稳定的重复性和可靠性;
3、吸附性能好,空白值低,孔底透明度高的固相载体;
4、适用血清、血浆、组织匀浆液、细胞培养上清液、尿液等等多种标本类型;
5、节省实验经费。
文章来源:http://www.abbkine.cn/elisa-assay-kit
联系邮箱:kefu@labbase.net
版权与免责声明
- 凡本网注明“来源:来宝网”的所有作品,版权均属于来宝网,转载请必须注明来宝网, https://www.labbase.net,违反者本网将追究相关法律责任。
- 本网转载并注明自其它来源的作品,目的在于传递更多信息,并不代表本网赞同其观点或证实其内容的真实性,不承担此类作品侵权行为的直接责任及连带责任。其他媒体、网站或个人从本网转载时,必须保留本网注明的作品来源,并自负版权等法律责任。
- 如涉及作品内容、版权等问题,请在作品发表之日起一周内与本网联系,否则视为放弃相关权利。