甲型肝炎病毒结构蛋白的分离纯化及鉴定
- 来宝网2007年6月14日 13:58 点击:4013
|
甲型肝炎病毒结构蛋白的分离纯化及鉴定
卢银平 林雨霖 姚学军 钱奇珍 李 晖 张蔚英
摘 要 利用高效持续带毒增殖的细胞株传代增殖获取甲型肝炎病毒(HAV)。采用不连续蔗糖/甘油密度梯度超速离心分离高度纯化的HAV颗粒。温和病毒裂解液裂解病毒后,运用高效液相色谱分离出三种蛋白,SDS-PAGE和Western-blot证实所分离蛋白为HAV三种主要结构蛋白VP1、VP2和VP3,蛋白含量较高。 关键词 甲型肝炎病毒,结构蛋白,分离,纯化,鉴定 Separation, Purification and Identification of Structural Proteins of Hepatitis A Virus Lu Yinping1 Lin Yulin2 Yao Xuejun2 Qin Qizhen2 Li Hui2 Zhang Weiying2 Abstract A cell line persistently infected by Hepatitis A virus (HAV) was ultilized to produce high yield viral particles of HAV. HAV particles were recovered in a single ultracentrifugation step through discontinuous sucrose/glycerol density gradients. Three kinds of major structural protein of HAV were separated and purified by high performance liquid chormatography. SDS-PAGE demonstrated the molecular weight of three structural proteins of HAV being 33, 29 and 27 kD. The special immune reactions were shown in Western-blot test, suggesting the proteins with 33, 29 and 27 kD are VP1, VP2 and VP3 of the virus, respectively. The total contents of the proteins, VP1, VP2 and VP3 were respectively 687, 220.8, 68 and 213.6 μg from 11 200 cm\+2 cells infected with HAV. The highly purified particles and sturctural proteins of HAV may be used in research for the development of vaccine, clinical diagnosis and pathogenesis of HAV. 甲型肝炎病毒的发病率在各型病毒性肝炎中仍居首位,然而HAV感染的始发机理一直都是亟待解决但尚未弄清楚的课题,至今没有阐明感染始发有关衣壳蛋白种类及各种衣壳蛋白在感染始发中的相互作用。因此有效分离出高度纯化和保持蛋白天然空间结构的HAV三种主要结构蛋白VP1、VP2和VP3,对研究解决HAV感染始发机理具有重要意义。国外有学者报道分离出几种HAV结构蛋白,但因实验中使用蛋白变性剂,所获蛋白为变性结构蛋白[1,2];国内尚未见到有关HAV结构蛋白分离纯化的报道。本研究采用超速离心和高效液相色谱技术,首次成功分离出具有蛋白本身天然结构的HAV的三种主要结构蛋白,旨在为解决HAV感染始发机制研究提供丰富材料和有力手段。 1 材料和方法 2 结果 |
|
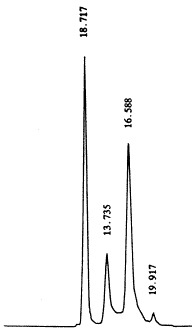
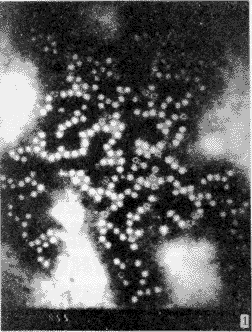
图1 负染免疫电镜照片。示超速离心后样品HAV被抗HAV McAb凝集成的病毒聚集体。 2.3 HPLC分离HAV结构蛋白及重复性 分离到三个大致呈正态分布的较窄的蛋白峰,保留时间分别为10.72 min、13.73 min、16.58 min(见图2),将收集到三个峰样品分别重新进样,各自得到一个峰,保留时间与原最初样品保留时间相对应。样品多次进样出峰和保留时间也无改变。
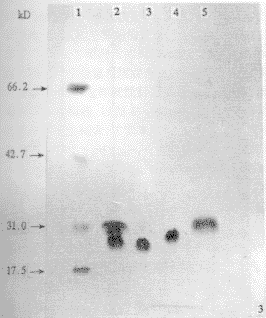
图2 高效液相色谱分离HAV结构蛋白三个洗脱峰。保留时间分别为10.72 min、13.73 min、16.58 min。 2.4 分子量测定 HAV结构蛋白分子量分别为33、29、27 kD;HPLC所得三个峰样品分子量:保留时间10.72 min的为33 kD;保留时间13.73 min的为29 kD;保留时间16.58 min的为27 kD(见图3)。 |
|
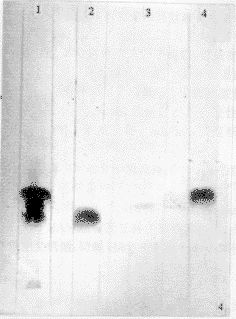
图3 SDS-PAGE照片。1.标准分子量; 2.HAV; 3.HPLC分离物(16.58 min); 4.HPLC分离物(13.73 min); 2.5 Western-blot鉴定各结构蛋白
图4 Western-blot,用HAV患者恢复期血清和羊抗人IgG-HRP反应系统。1.HAV; 2. 27 kD蛋白(16.58 min峰);3. 29 kD蛋白(13.73 min峰);4.33 kD蛋白(10.72 min峰)。 2.5.2 用抗HAV VP1 McAb bF4和羊抗鼠IgG-HRP分别作一抗和二抗,超速离心HAV样品出现分子量为33 kD一条带,而HPLC收集到的三个峰样品仅见保留时间为10.72 min(33 kD)者出现阳性条带,其它二峰值样品为阴性反应,未见条带(见图5),证明保留时间为10.72 min的蛋白是HAV结构蛋白VP1。 |
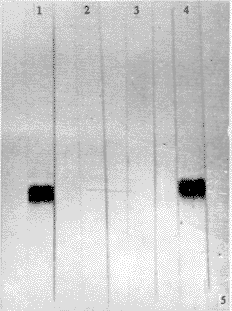
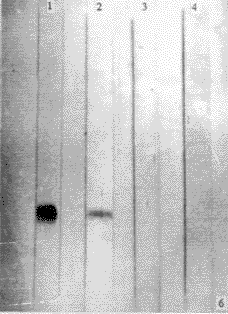
| 图5 Western-blot。用抗HAV VP1单抗bF4和羊抗鼠IgG-HRP反应系统。1.HAV; 2.27 kD蛋白(16.58 min峰); 3. 29 kD蛋白(13.73 min峰); 4. 33 kD蛋白(10.72 min峰)。 Fig.5 Western-blot analysis of McAb against HAV VP1 with complete virions (Lane 1) and HPLC purified structural proteins of HAV(Lane 2 to 4). 2.5.3 用抗HAV VP3 McAb 3D9和 羊抗鼠IgG-HRP分别作一抗和二抗,超速离心HAV颗粒出现分子量为27 kD一条带,HPLC收集的样品仅见保留时间为16.58 min的峰(27 kD)处者出现一条带,其它二峰未见条带(见图6),证明保留时间为16.58 min的蛋白(27 kD)为HAV结构蛋白VP3。
Fig.6 Western-blot analysis of McAb against HAV VP3 with complete virions (Lane 1) and HPLC purified structural proteins of HAV(Lane 2 to 4). 2.5.4 HPLC收集的保留时间为13.73 min (29 kD)样品能与HAV患者恢复期血清发生免疫反应,而不能与抗HAV VP3、VP1单克隆抗体发生免疫反应,证明它为HAV另一种结构蛋白VP2,其分子量与文献报道分子量[2]相吻合。 3 讨论 致谢 本实验得到中科院武汉病毒所唐建客老师及湖北医科大学实验中心崔冶建老师大力支持,在此表示衷心感谢! 作者单位:卢银平 同济医科大学附属协和医院病毒室,武汉 430022 参考文献 |
联系邮箱:kefu@labbase.net
版权与免责声明
- 凡本网注明“来源:来宝网”的所有作品,版权均属于来宝网,转载请必须注明来宝网, http://www.labbase.net,违反者本网将追究相关法律责任。
- 本网转载并注明自其它来源的作品,目的在于传递更多信息,并不代表本网赞同其观点或证实其内容的真实性,不承担此类作品侵权行为的直接责任及连带责任。其他媒体、网站或个人从本网转载时,必须保留本网注明的作品来源,并自负版权等法律责任。
- 如涉及作品内容、版权等问题,请在作品发表之日起一周内与本网联系,否则视为放弃相关权利。