君实生物拓益鼻咽癌一线适应症全国上市会在广州举办
- 美通社2022年2月6日 11:13 点击:521
“鼻此共拓,益未来”
上海2022年1月24日 /美通社/ -- 2022年1月22日,“鼻此共拓,益未来”CSCO-君实生物拓益®(特瑞普利单抗注射液)鼻咽癌一线适应症全国上市会,以线上线下、主会分会相结合的形式在广州顺利举办。中山大学肿瘤防治中心徐瑞华教授和卢泰祥教授,福建省肿瘤医院潘建基教授担任大会名誉主席;中山大学肿瘤防治中心马骏教授、复旦大学附属肿瘤医院胡超苏教授、中山大学肿瘤防治中心麦海强教授共同担任大会主席;浙江省肿瘤医院陈晓钟教授、福建省肿瘤医院林少俊教授、贵州省肿瘤医院金风教授、中山大学肿瘤防治中心赵充教授任分会主席。中国临床肿瘤协会(CSCO)鼻咽癌、头颈部肿瘤领域众多专家学者与会,共同庆祝拓益®鼻咽癌一线适应症上市,并围绕新兴免疫治疗在鼻咽癌领域的成果与前景展开了深入探讨。
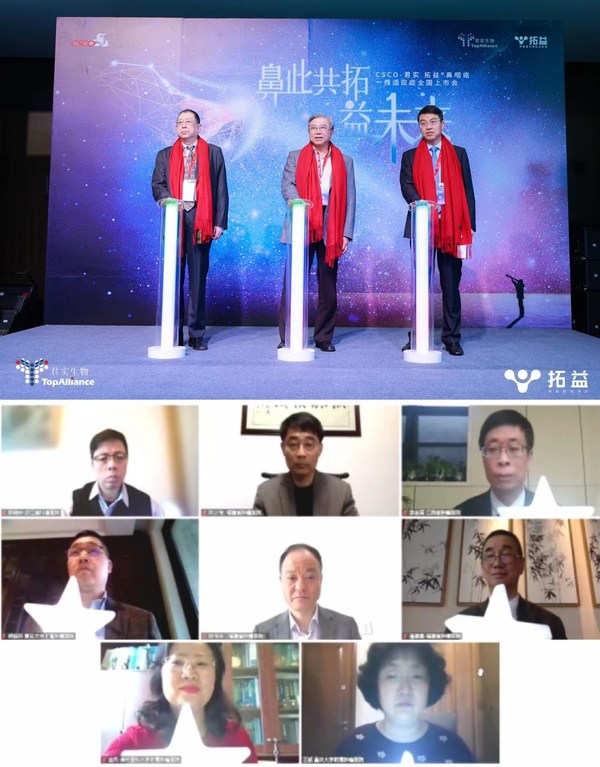
拓益®鼻咽癌一线适应症全国上市会启动&拓益®治疗鼻咽癌纳入国家医保目录庆祝仪式 线下仪式嘉宾:马骏教授、卢泰祥教授、李聪先生; 线上仪式嘉宾:陈传本教授(福建省肿瘤医院)、陈晓钟教授、胡超苏教授、金风教授、李金高教授(江西省肿瘤医院)、林少俊教授、潘建基教授、王颖教授(重庆大学附属肿瘤医院)
特瑞普利单抗是由中国生物医药创新“先行者”君实生物自主研发的重组人源化抗PD-1单克隆抗体注射液,是全球首个获批鼻咽癌治疗的免疫检查点抑制剂,实现了鼻咽癌治疗领域免疫治疗零的突破。此次上市的拓益®鼻咽癌一线适应症为特瑞普利单抗联合顺铂和吉西他滨用于局部复发或转移性鼻咽癌患者的一线治疗,这也是拓益®在鼻咽癌领域获批上市的第二项适应症,不但为该领域患者带来了前沿的肿瘤免疫疗法,助力中国创新成果造福国人,也在国际上引领了鼻咽癌领域的诊疗发展。
“鼻咽癌是一个比较特殊的肿瘤类型,全球范围内来看,我国是绝对的高发地区。在这个领域,目前我国的诊疗和研究水平均处在世界前列,让中国患者率先受益于创新疗法,也是我们研究者义不容辞的责任。”大会名誉主席徐瑞华教授致辞称。
大会名誉主席潘建基教授表示:“随着抗肿瘤新药的研发和临床治疗新技术的出现,鼻咽癌治疗格局在近年来迎来了变革性的突破。希望君实生物能继续投入研发创新,推动我国抗肿瘤事业的不断发展,提高临床医生的肿瘤诊治水平,改善我国癌症患者的生存。”
与上市会一同举办的,还有拓益®治疗鼻咽癌纳入国家医保目录庆祝仪式。2022年1月1日,新版国家医保药品目录实施,特瑞普利单抗成为目录中唯一用于鼻咽癌治疗的抗PD-1单抗,有望让更广大患者受益于创新疗法。
大会名誉主席卢泰祥教授致辞道:“此次拓益®在鼻咽癌一线治疗‘再下一城’,将为处于不同疾病阶段的患者带来创新的治疗方案和更长的生存获益。目前拓益®治疗晚期鼻咽癌已纳入2021版国家医保目录,可及性更高,将造福更多中国患者!”
定义晚期鼻咽癌全线免疫治疗新标准
拓益®鼻咽癌一线适应症获批基于的JUPITER-02研究,是一项随机、双盲、安慰剂对照、国际多中心的免疫治疗联合标准化疗一线治疗复发/转移性鼻咽癌的Ⅲ期临床研究,由徐瑞华教授担任主要研究者,在中国、美国两地同时注册,共纳入289例未接受过化疗的复发/转移性鼻咽癌患者。
会上,麦海强教授对JUPITER-02研究亮点着重进行了介绍:“目前临床应用的局部复发或转移性鼻咽癌患者一线治疗手段,疗效不够理想,因此,亟需探索更为有效的治疗方案。JUPITER-02研究有人群涵盖更广,P值、HR值双认证,疗效指标全面获益三大特点。通过JUPITER-02研究,我们欣喜地看到,与单纯化疗相比,特瑞普利单抗联合吉西他滨和顺铂(GP化疗)一线治疗复发/转移性鼻咽癌可获得更优的无进展生存期(PFS)、更高的客观缓解率(ORR)和更长的缓解持续时间(DoR),安全性可管理。”
麦海强教授具体分析道,研究结果显示,特瑞普利单抗组主要研究终点PFS(BIRC评估)达11.7个月,比化疗组延长3.7个月,死亡风险或疾病进展风险比化疗组降低48%;两组的OS数据尚未成熟,但特瑞普利单抗组OS显著延长,死亡风险降低了40%。
值得一提的是,此项研究多次获得国际学界高度认可,曾以“重磅研究摘要”(#LBA2)形式入选美国临床肿瘤学会年会(ASCO 2021)全体大会,并荣登国际顶尖期刊《自然-医学》杂志(Nature Medicine,影响因子:53.440)封面,这也是《自然-医学》创刊26年来首次在封面上推荐中国创新药物研究。
历经5年时间,从Ib/II期的小样本量探索性研究、II期免疫单药二线及后线治疗的POLARIS-02研究,到首创全球迄今为止规模最大的国际多中心“免疫治疗+化疗”一线治疗的JUPITER-02研究,研发团队实现了对晚期鼻咽癌后线至一线临床布局的“全线贯穿”。“特瑞普利单抗改写了2021版《CSCO鼻咽癌诊疗指南》,在一线、二线及以上、三线及以上治疗中均得到专家推荐。目前,特瑞普利单抗的多项研究都在全力推进。在鼻咽癌治疗领域,‘中国力量’改变了世界,重塑了鼻咽癌治疗标准,我们期待特瑞普利单抗在鼻咽癌领域发出更多的好声音。”麦海强教授表示。
让“中国方案”造福全球患者
以往国际上以PD-1为代表的免疫治疗药物适应症的开发主要围绕欧美主流病症,像鼻咽癌这类亚洲高发瘤种则长期被忽视。作为本土创新药企,君实生物积极携手中国专家学者,大胆探索创新,旨在满足中国患者长期未被满足的临床需求。
君实生物高级副总裁姚盛博士在上市会上表示:“君实生物持续关注国人中高发,且对免疫治疗有较好响应、临床急需治疗的瘤种。全球近半数的鼻咽癌新发病例在中国,但治疗手段的开发在全球层面长期滞后。我们先后开展POLARIS-02和JUPITER-02两项研究,力求改变复发转移性鼻咽癌患者的境遇。让我们感到欣慰的是,特瑞普利成功验证了免疫单药与化疗联合治疗在该领域的有效性,为患者提供了更好的治疗选择。”
在“立足中国,布局全球”战略指引下,君实生物正努力让“中国方案”造福全球患者。基于特瑞普利单抗在POLARIS-02和JUPITER-02两项研究中取得的卓越成果,美国食品药品监督管理局(FDA)已授予该药品2项突破性疗法认定,旨在加速其开发和审评程序。目前,君实生物已向FDA提交了特瑞普利单抗联合吉西他滨/顺铂作为晚期复发或转移性鼻咽癌患者的一线治疗和单药用于复发或转移性鼻咽癌含铂治疗后的二线及以上治疗的两项适应症的生物制品许可申请(BLA)并获受理,特瑞普利单抗也是首个向FDA提交上市申请的国产抗PD-1单抗。
君实生物联席首席执行官李聪先生表示:“在鼻咽癌领域,特瑞普利单抗已相继取得两项适应症上市,其中后线治疗适应症已通过2021年国谈被纳入医保,这必将满足更多中国鼻咽癌患者的需求。与此同时,我们也正在全球层面积极推进特瑞普利单抗等创新药物的研发与商业化工作,推动中国本土创新药物走向世界,普惠全球患者。”
关于鼻咽癌
鼻咽癌是一种发生于鼻咽部黏膜上皮的恶性肿瘤,是常见的头颈部恶性肿瘤之一。据世界卫生组织统计,2020年鼻咽癌在全球范围内确诊的新发病例数超过13万。对于复发或转移性鼻咽癌,目前的治疗手段有限,一线标准治疗方案是吉西他滨联合顺铂化疗,患者的总体生存亟待改善。对于一线含铂类化疗失败的患者目前仍缺乏标准的后线治疗方案。
关于特瑞普利单抗注射液(拓益®)
特瑞普利单抗注射液(拓益®)作为我国批准上市的首个国产以PD-1为靶点的单抗药物,获得国家科技重大专项项目支持。本品获批的第一个适应症为用于既往接受全身系统治疗失败的不可切除或转移性黑色素瘤的治疗。2020年12月,特瑞普利单抗首次通过国家医保谈判,目前已有3项适应症纳入《2021年药品目录》。2021年2月,特瑞普利单抗获得国家药品监督管理局(NMPA)批准,用于既往接受过二线及以上系统治疗失败的复发/转移性鼻咽癌患者的治疗。2021年4月,特瑞普利单抗获得NMPA批准,用于含铂化疗失败包括新辅助或辅助化疗12个月内进展的局部晚期或转移性尿路上皮癌的治疗。2021年11月,特瑞普利单抗联合顺铂和吉西他滨用于局部复发或转移性鼻咽癌患者的一线治疗的新适应症获得NMPA批准。此外,特瑞普利单抗还获得了《中国临床肿瘤学会(CSCO)黑色素瘤诊疗指南》、《CSCO头颈部肿瘤诊疗指南》、《CSCO鼻咽癌诊疗指南》、《CSCO尿路上皮癌诊疗指南》及《CSCO免疫检查点抑制剂临床应用指南》推荐。
2021年3月,特瑞普利单抗用于晚期黏膜黑色素瘤的一线治疗被国家药监局纳入突破性治疗药物程序。2021年7月,特瑞普利单抗联合含铂化疗一线治疗局部晚期或转移性食管鳞癌的新适应症上市申请获得NMPA受理。2021年12月,特瑞普利单抗联合标准一线化疗用于未经治疗、驱动基因阴性的晚期非小细胞肺癌的新适应症上市申请获得NMPA受理。在国际化布局方面,特瑞普利单抗在美国食品药品监督管理局(FDA)的首个上市申请(BLA)已获受理并被授予优先审评,特瑞普利单抗也是首个向FDA提交BLA的国产抗PD-1单抗。目前,特瑞普利单抗已在黏膜黑色素瘤、鼻咽癌、软组织肉瘤、食管癌领域获得FDA授予2项突破性疗法认定、1项快速通道认定、1项优先审评认定和4项孤儿药资格认定。
特瑞普利单抗自2016年初开始临床研发,至今已在全球开展了覆盖超过15个适应症的30多项临床研究,积极探索本品在黑色素瘤、鼻咽癌、尿路上皮癌、肺癌、胃癌、食管癌、肝癌、胆管癌、乳腺癌、肾癌等适应症的疗效和安全性,与国内外领先创新药企的联合疗法合作也在进行当中,期待让更多中国以及其它国家的患者获得国际先进水平的肿瘤免疫治疗。
关于君实生物
君实生物(688180.SH,1877.HK)成立于2012年12月,是一家以创新为驱动,致力于创新疗法的发现、开发和商业化的生物制药公司。公司具有由45项在研产品组成的丰富的研发管线,覆盖五大治疗领域,包括恶性肿瘤、自身免疫系统疾病、慢性代谢类疾病、神经系统类疾病以及感染性疾病。
凭借蛋白质工程核心平台技术,君实生物身处国际大分子药物研发前沿,获得了首个国产抗PD-1单克隆抗体NMPA上市批准、国产抗PCSK9单克隆抗体NMPA临床申请批准、全球首个治疗肿瘤抗BTLA阻断抗体在中国NMPA和美国FDA的临床申请批准,在中美两地进行I期临床研究。2020年,君实生物还与国内科研机构携手抗疫,共同开发的JS016已作为国内首个抗新冠病毒单克隆中和抗体进入临床试验,目前已在全球超过15个国家和地区获得紧急使用授权,用本土创新为中国和世界疾病预防控制贡献力量。目前君实生物在全球拥有两千五百多名员工,分布在美国旧金山和马里兰,中国上海、苏州、北京和广州。
官方网站:www.junshipharma.com
官方微信:君实生物
联系邮箱:kefu@labbase.net
版权与免责声明
- 凡本网注明“来源:来宝网”的所有作品,版权均属于来宝网,转载请必须注明来宝网, http://www.labbase.net,违反者本网将追究相关法律责任。
- 本网转载并注明自其它来源的作品,目的在于传递更多信息,并不代表本网赞同其观点或证实其内容的真实性,不承担此类作品侵权行为的直接责任及连带责任。其他媒体、网站或个人从本网转载时,必须保留本网注明的作品来源,并自负版权等法律责任。
- 如涉及作品内容、版权等问题,请在作品发表之日起一周内与本网联系,否则视为放弃相关权利。